分子检测定性项目的性能验证 - HLA基因检测新闻
为加强新冠病毒核酸检测能力建设,以更好满足新冠肺炎疫情常态化防控要求,去年至今各地新建和改扩建的PCR实验室数量快速增长。虽在每次举办的PCR培训班上我们都会重点讲解性能验证相关内容,但在实验室现场验收或督查过程中,仍发现不少实验室对性能验证相关知识并不是很清楚。今天就以新冠病毒核酸检测项目为例,和大家探讨一下分子检测定性项目性能验证的一些知识,希望能对大家有点帮助。
检验程序常规应用前。 任何严重影响检测系统分析性能的情况发生后(包括但不限于仪器主要部件故障、仪器搬迁、设施环境的严重失控等),应在检测系统重新启用前对受影响的性能进行部分性能验证。 实验室增加新的检测系统时,新的检测系统包含现用检测系统的任一要素(仪器、试剂等)变更,如试剂升级、仪器更新等。
PS:新增检测项目时需做性能验证,大部分实验室都很清楚这点。但有些实验室在新增/变更部分仪器/试剂的情况下,认为仅进行系统间比对即可,这并不符合相关要求,此种情况下也是需按照新系统进行性能验证。
操作人员应经过培训,熟悉所用方法原理与操作。 仪器经过校准,各项性能指标合格。 实验室设施及环境符合工作要求。 试剂满足要求。 性能验证人员应了解验证方案、制定验证计划并组织实施。
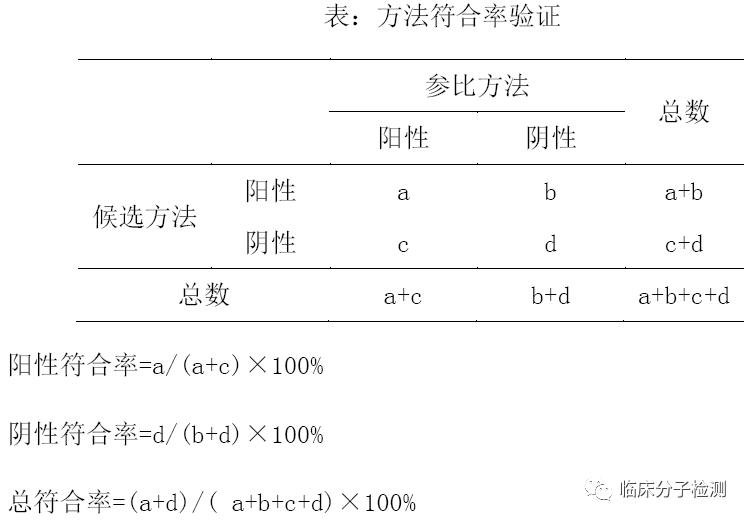
验证要求:通过与参比方法进行比较。参比方法:金标准方法、行业公认方法、经验证性能符合要求满足临床预期用途的方法(如:通过 ISO15189 认可实验室使用的相同检测方法)。 验证方案:
样本:新鲜或冻存的阴性和弱阳性样本各一份。对于无法获得足量临床阳性样本的项目,可对临床阳性样本进行稀释或使用人工制备样本(如假病毒颗粒、质粒等)。 验证方法:每天检测3-4次,连续检测5天,阴阳性样本符合率≥90%。如对新冠病毒核酸检测项目,其阴阳性样本的符合率应为100%,同时阳性样本重复检测Ct值的变异系数(CV)应<5%。
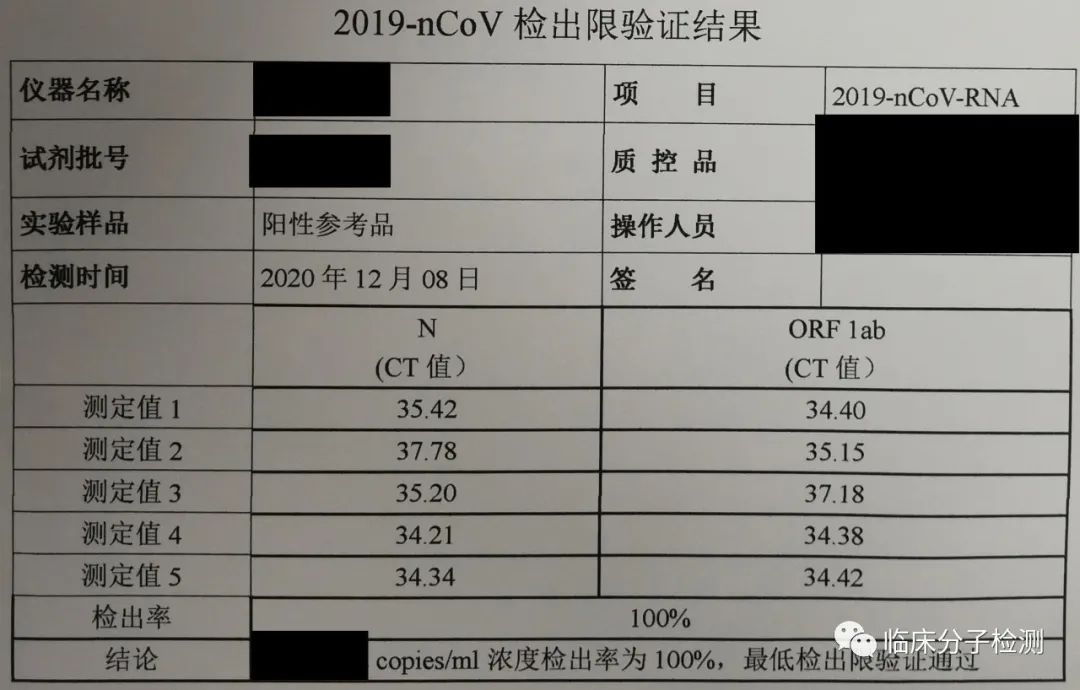
验证要求:所用检验程序在厂家试剂使用说明书等有声明检出限时,检测项目在有标准物质时,或以定量形式表达定性结果时,应进行检出限的验证。 样本要求:定值标准物质(如:国际参考品、国家参考品、厂家参考品)。对于报告具体基因型的方法,其选用的标准物质需包括所有的突变类型。对于检测对象同时含有不同比例的不同基因型时,应设置多个梯度,主要从扩增反应终体系总核酸浓度和突变序列所占比例两个方面进行评价。 验证方法:使用定值标准物质的样本梯度稀释至厂家声明的检出限浓度,可重复测定5次或在不同批内对该浓度样本进行20次重复测定(如测定5天,每天测定4份样本)。稀释液可根据情况选用厂家提供的稀释液或阴性血清,该阴性血清除被验证的目标物必须阴性外,所含干扰物质浓度必须在厂家声明的范围之内。如对于新冠病毒核酸检测项目,可选用有证的定值标准物质或定值质控品样本。 判断标准:如果是5次重复检测,必须100%检出靶核酸;如果是20次检测,必须检出至少18次靶核酸。
当然,除上述符合率、精密度和检出限等性能指标外,实验室也可根据自身情况对试剂说明书中的其他性能指标进行验证,如交叉反应和抗干扰能力等,不过这并不是强制要求的。
从定性结果来看,此浓度样本确实100%检出了。但如果仔细看下N基因和ORF1ab基因检测的Ct值,我想很多人应该会产生这样的疑问:这是同一浓度样本同批重复5次的检测结果?如果真的做成这样,那说明检测系统中某个环节必然存在大问题!而如果检测系统没有问题,那么只能说明这份报告并不真实。
因此,为保证实验室检测系统良好运行,请大家务必认真对待性能验证,严格按照相关要求进行性能验证,以最大限度地保证本实验室检测结果的准确可靠。
CNAS-CL02:2012《医学实验室质量和能力认可准则》
CNAS-GL039:2019《分子诊断检验程序性能验证指南》
CNAS-GL037:2019《临床化学定量检验程序性能验证指南》
声明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 邮箱地址:2513零1765#qq.com
==========================================================
您可能喜欢的内容
==========================================================
泌尿生殖道病原体核酸(RNA)检测 - HLA基因检测新闻
一、他们是什么?这4个家伙分别是 沙眼衣原体(CT)淋病奈瑟菌(NG)解脲脲原体(UU)生殖支原体(MG);CT/NG/UU/MG均是泌尿生殖道感染常见病原体,其中:①淋病奈瑟菌(NG)引起的泌尿生殖系统化脓性感染,是常见的性传播疾病之一;可引发男性淋菌性尿道炎、女性淋菌性尿道炎和宫颈炎②非淋菌性尿道炎(NGU)则与支原体、衣原体相关。二、筛查推荐l美国疾控中心(US CDC)、美国预防服务工作组(USPSTF) 、英国国家临床最优化研究所(NICE)指南均推荐所有育龄人群中进行CT或NG检查;l中国2014版 《梅毒、淋病、生殖器疱疹、生殖道沙眼衣原体感染诊疗指南》 推荐采取SAT方法检测病原体RNA;lRNA方法检测较传统培养,DNA检测方法,在保证灵敏度高,不易漏检的同时,可有效区分死菌或活菌(可进行疗效评估和 ...
2019检测机构报告出炉!三大区域检测机构营收占比超80% - HLA基因检测新闻
截至2019年底,我国共有检验检测机构44007家,2019全年实现营业收入3225.09亿元。 从检测机构区域分布来看,华东地区占比27.49%,华北地区占比17.43%,中南地区占比24.29%,三大区域占比合计69.21%。从省份分布来看,山东、广东和江苏检测机构数量排名前三。 从检测机构营业收入的区域比重来看,华东地区占比35.58%、华北地区占比17.85%、中南地区占比26.71%,三大区域占比合计80.14%。从省份分布来看,广东、上海和江苏检测机构营业收入排名前三。 检验检测机构数量及检验检测市场规模同步增长 2015-2019年,我国检测行业持续扩容,根据国家市场监管总局统计,截至2019年底,我国境内(不含港澳台)检验检测服务业共有检验检测机构44007家,较2018年增长11.49% ...
总磷检测的注意事项 - HLA基因检测新闻
二代COD氨氮总磷总氮检测仪测定总磷用的是国标的钼氨酸法。今天我给大家讲解一下总磷检测时需要注意的一些事项:1.总磷很容易吸附在塑料瓶上,因此我们采样时尽可能的是用玻璃瓶,而且取样需要是现取现用,如果不能及时检测应该用硫酸酸化至水样PH小于2,检测前需要调节PH至中性;2.总磷试剂B为抗坏血酸。一定要保存在4度左右的冰箱里,否则会失效,判断的依据是试剂的颜色,变黄说明试剂失效,而且在加入试剂前试管必须完全冷却下来;3.检测的水样消解后必须要澄清,如果水样消解后有颜色说明干扰比较大;我们的仪器的处理方法就是稀释水样,有条件的可以做色度补偿;4.加入显色剂后要注意控制显色时间,15分钟为好;夏天温度在25度以上显色10分钟左右,冬天温度低可以在20-30度水浴加热显色,尽量控制在15分钟左右;显色时间过长总磷的值会下降。 ...
我国现行真菌毒素检测标准概述 - HLA基因检测新闻
1 真菌毒素标准的发展 真菌毒素是产毒真菌在粮食(或果蔬)的种植、收获、运输、储存过程中侵染粮食(或果蔬),并在适宜的生长条件下产生的次生代谢产物。真菌毒素污染谷物、饲料、果蔬,通过食物链危害人类健康和畜禽生产安全。因此,世界卫生组织(World Health Organization,WHO)和联合国粮农组织(Food and Agriculture Organization,FAO)把真菌毒素列为食源性疾病的三大根源之首。我国是真菌毒素污染最严重的国家之一。 目前,人们发现的真菌毒素有400多种。我国重点关注黄曲霉毒素(主要是Aflatoxin B1,AFB1和Aflatoxin M1,AFM1)、脱氧雪腐镰刀菌烯醇(Deoxynivalenol,DON)、玉米赤霉烯酮(Zearalenone,ZEN)、赭曲 ...
新冠病毒核酸检测原理是什么 - HLA基因检测新闻
核酸检测的物质是病毒的核酸。核酸检测是查找患者的呼吸道标本、血液或粪便中是否存在外来入侵的病毒的核酸,来确定是否被新冠病毒感染。因此一旦检测为核酸“阳性”,即可证明患者体内有病毒存在。 新冠病毒感染人体之后,首先会在呼吸道系统中进行繁殖,因此可以通过检测痰液、鼻咽拭子中的病毒核酸判断人体是否感染病毒。所以说,核酸检测阳性可以作为新型冠状病毒感染确诊的新标准。 检测新型冠状病毒特异序列的方法最常见的是荧光定量PCR(聚合酶链式反应)。因PCR反应模板仅为DNA,因此在进行PCR反应前,应将新型冠状病毒核酸(RNA)逆转录为DNA。在PCR反应体系中,包含一对特异性引物以及一个Taqman探针,该探针为一段特异性寡核苷酸序列,两端分别标记了报告荧光基团和淬灭荧光基团。探针完整时,报告基团发射的荧光信号被淬灭基团吸 ...
一文详解pdl1检测 - HLA基因检测新闻
在今年NCCN指南中明确提出对于无明确驱动基因突变的初诊的晚期NSCLC肺癌患者可以进行PD-L1的检测,如果PD-L1表达≥50%,初始治疗可以选择PD-1单抗Keytruda用药。基于其较化疗优越的临床生存优势及较少的不良反应。很多医生及患者朋友们也意识到,一线使用Keytruda重点在筛查相应人群,而PD-L1表达≥50%的人群占整体晚期NSCLC的27%左右。那PD-L1检测如何去做呢? 自肺癌治疗格局改变后,免疫治疗作为一种新的治疗方法逐渐被大家所认知。每天关于免疫治疗的知识更新也在不断传播。但当这一治疗落实到临床实践中时,就提出了很多的问题。今日我们就近期很多患者提到的PD-L1的检测进行简单的解析。 在今年NCCN指南中明确提出对于无明确驱动基因突变的初诊的晚期NSCLC肺癌患者可以进行PD-L ...
马上开始检测,获得精准资料
免费获取方案 →